واحد تضمین کیفیت، مسئول فنی و رگولاتوری؛
اولین و مهمترین اولویت شرکت داروسازی مداوا، اطمینان از سلامت و ایمنی بیمار می باشد. وظیفه واحد "تضمین کیفیت" (Quality Assurance یا QA) اطمینان از استقرار یک سیستم تحت کنترل و حفظ آن است؛ وضعیت تحت کنترل به معنی تضمین کیفیت، سلامت و خلوص محصول در کل پروسه تولید می باشد.
هدف واحد "تضمین کیفیت" این است که به طور فعالانه از تولید محصول نامنطبق جلوگیری کند.
تفاوت واحد "کنترل کیفیت" و "تضمین کیفیت":
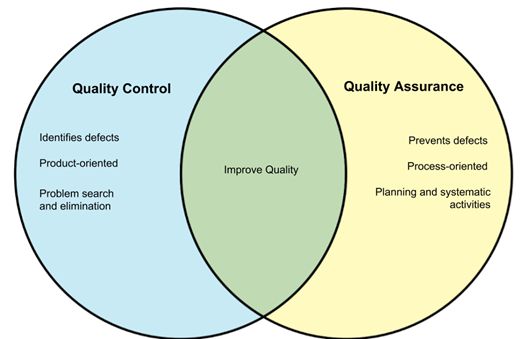
تضمین کیفیت (QA)، مجموعه عملیات و فعالیت های پیشگیرانه و آینده نگری است که اطمینان لازم مبنی بر برآورده سازی الزامات را به دست می دهد. در حالی که کنترل کیفیت (QC)، عملیات و فعالیت های حین مراحل فیزیکی ساخت کالا است که اطمینان حاصل می کند محصولات تولیدی به صورتی تکرار پذیر، مشخصات و ویژگی های لازم را دارا می باشند.
تضمین کیفیت (QA) بیشتر فرآیند محور بوده و از وقوع خطاها، نقایص و اشتباه ها جلوگیری می کند. در حالی که کنترل کیفیت (QC)محصول محور است و وقوع خطاها، نقایص و اشتباه ها را کشف میکند.
شرح وظایف تضمین کیفیت (QA)، مسئول فنی (QP) و رگولاتوری به طور مختصر ؛
1. فرآیند آزاد سازی محصولات تمام شده؛
1.1. تمام پروسه تولید هر سری ساخت از هر محصولی به طور کامل مستند می شود و قابل ردیابی است.
1.2. مسئول فنی با دانش بر الزامات کیفی و قانونی، مسئولیت آزادسازی محصولات را بر عهده دارد.
2. مدیریت ریسک های کیفی؛
2.1. شناسایی ریسک ها و خطرات کیفی احتمالی در تمام پروسه ها ، تجهیزات و ساختمان ها و ارائه راهکار جهت به حداقل رساندن آن ها.
3. مدیریت تامین کنندگان و پیمانکاران
3.1. تمامی تامین کننده ها اعم از تامین کننده های مواد اولیه دارویی، ملزومات بسته بندی، شرکت های پخش و شرکت های ارائه دهنده خدمات، مانند کالیبراسیون، بایستی طی یک برنامه جامع ارزیابی و امتیاز دهی شوند.
3.2. در صورت تایید مسئول فنی و مدیر تضمین کیفیت مجوز همکاری صادر می شود.
4. اعتبارسنجی و کالیبراسیون؛
4.1. اثبات مستند انطباق نتایج به دست آمده از یک روش، فرآیند، ماده، فعالیت، سیستم یا دستگاه با نتایج مورد انتظار می باشد.
5. بازرسی داخلی؛
5.1. بازرسی دوره ای تمامی واحدهای اجرایی برای حصول اطمینان از انطباق فرآیندهای جاری در کارخانه با اصول GXP، بهبود مستمر کیفی در کارخانه و کاهش هزینه ها ( با بازرسی موثر) در راستای بهینه سازی محصولات تولیدی توسط واحد تضمین کیفیت انجام می شود.
6. مدیریت مستندات؛
6.1. مستندات و مستندسازی خوب بخش مهم و ضروری از سیستم تضمین کیفیت است، لذا کلیه عملیات و فعالیت ها بایستی مستند و قابل ردیابی باشند.
6.2. نوشتن واضح مستندات از بروز خطاهای ناشی از ارتباطات شفاهی جلوگیری نموده و امکان پیگیری سوابق هر سری ساخت محصول را فراهم مینماید.
6.3. هدف اصلی سیستم مستندسازی، کنترل، پایش و ثبت کلیه فعالیتهایی که بطور مستقیم یا غیر مستقیم برروی همه جنبه های کیفی فرآورده های دارویی اثر میگذارد.
7. آموزش؛
7.1.برای تمامی پرسنل شرکت به طور مداوم نیاز سنجی آموزشی انجام شده و متناسب با شرح وظایف فرد، آموزش های لازم برای وی در نظر گرفته می شود.
8. مدیریت عدم انطباق و اقدامات اصلاحی
8.1. شناسایی رویدادهای کیفی، ارائه راهکار جهت اصلاح آن و پیشگیری از وقوع مجدد.
9. مدیریت تغییرات
9.1. هرگونه تغییری در پروسه تولید، دستگاه ها، پرسنل کلیدی و ... باید پیش از اجرا، به صورت مکتوب به واحد تضمین کیفیت اعلام شود.
9.2. مدیر تضمین کیفیت و مسئول فنی پس از ارزیابی کامل تغییرات پیشنهادی و ریسک های احتمالی، این تغییرات را تایید و یا رد می نمایند.
10. رسیدگی به شکایات؛
10.1. در راستای بهبود مستمر، هرگونه شکایت از طرف مصرف کننده و یا کادر پزشکی در خصوص محصولات مداوا، به طور کامل بررسی می شوند و مسئول فنی در خصوص آن محصول تصمیم گیری مینماید.
11. اقدامات رگولاتوری؛
11.1. اخذ پروانه ساخت محصولات جدید و تمدید و اصلاح پروانه ساخت محصولات قدیمی
11.2. قیمت گذاری محصولات جدید
11.3. هماهنگی جهت امحاء ضایعات دارویی و شیمیایی شرکت
12. بازبینی دوره محصول؛
12.1. به منظور اطمینان از تولید محصولات با کیفیت ثابت، سالانه تمامی محصولات تولید شده در سال گذشته مورد ارزیابی و بازبینی قرار میگیرند و روند نتایج بررسی و مقایسه می شود.
13. کنترل کیفیت محصولات در سطح عرضه (Product Quality Review یا PMQC)؛
13.1. شرکت های داروسازی موظف هستند نه تنها از حصول کیفیت مناسب محصولات در زمان آزادسازی اطمینان حاصل کنند، بلکه بایستی تداوم کیفیت در طول عمر قفسه دارو را نیز تضمین نمایند. بدین منظور یک یا چند محصول جهت بررسی و آنالیز انتخاب می شوند.
13.2. به دلیل تنوع شرایط اقلیمی کشور، به صورت دوره ای حداقل از 3 مختلف منطقه آب و هوایی کشور، محصول انتخابی نمونه برداری و آنالیز می شود.
14. فارماکوویژیلانس؛
14.1. فارماکوویژیلانس همچنین به عنوان ایمنی دارو (drug safety) نیز شناخته می شود.
14.2. دانشی است در خصوص جمع آوری، تشخیص، ارزیابی، کنترل و پیشگیری از عوارض جانبی محصولات دارویی که توسط پرسنل ذی صلاح و آموزش دیده، به کار گرفته می شود.
14.3. اطلاعات تماس با این دپارتمان در برگه های راهنمای محصولات مداوا ذکر شده است و بیماران و همکاران کادر درمان میتوانند جهت گزارش عوارض جانبی با این شرکت تماس حاصل نمایند.